Dessa forma, os EUA podem contar em dezembro com duas vacinas autorizadas para uso emergencial, que somarão 60 milhões de doses. Em 2021, o governo norte-americano pode ter acesso a mais de 1 bilhão de doses das fabricantes, volume que representa o triplo do necessário para a população do país, de 330 milhões.
O co-fundador da companhia alemã BioNTech, Ugur Sahin, no entanto, revelou que o impacto das vacinas contra a covid-19 vai crescer rapidamente na metade de 2021. Com isso, a vida só deve voltar ao normal no fim do próximo ano.
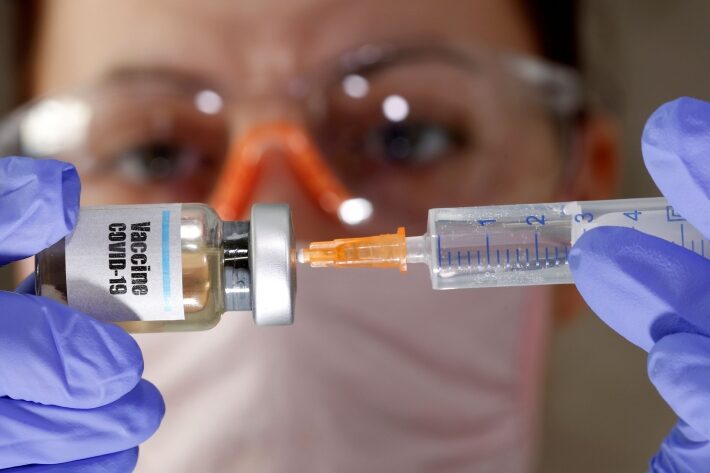
Desenvolvidas com uma nova tecnologia conhecida como RNA mensageiro, ou mRNA, as vacinas da Moderna e da Pfizer representam poderosas novas ferramentas para combater a pandemia. Até agora, o novo coronavírus infectou 54 milhões de pessoas em todo o mundo e matou 1,3 milhão. A notícia vem em um momento de alta de novos casos da doença, o que obriga países europeus a voltarem a impor lockdowns. Os Estados Unidos, por sua vez, atingem novos patamares recordes de infecção.
“Vamos fazer uma vacina para parar a covid-19”, disse o presidente da Moderna, Stephen Hoge. Uma vantagem crucial da vacina da Moderna é não exigir o armazenamento ultrafrio, como a da Pfizer, o que torna muito mais fácil a sua distribuição. A Moderna acredita que o imunizante se mantém estável em temperaturas típicas de geladeira (entre 2º e 8º Celsius) durante 30 dias, e pode ser armazenado por até seis meses a 20º C negativos.
A vacina da Pfizer, por sua vez, precisa ser transportada e armazenada a 70º C negativos. Sob temperaturas típicas de geladeira, ela pode ser armazenada por até cinco dias.
O teste com 30 mil participantes realizado pela Moderna apontou que a vacina evitou casos graves de covid-19, uma questão ainda não respondida pelo imunizante da Pfizer. Dos 95 casos do teste da Moderna, 11 foram graves e todos ocorreram entre voluntários que receberam o placebo.
Integrante da Operação Warp Speed do governo norte-americano, a Moderna espera produzir cerca de 20 milhões de doses da vacina para os EUA neste ano. Grande parte deste volume já está fabricado e pronto para ser distribuído, a partir da autorização da Agência de Alimentos e Medicamentos dos EUA (FDA).
“Assim que recebermos uma autorização de uso emergencial, estaremos prontos para despachar praticamente em questão de horas por meio do programa Warp Speed”, disse Hoge. “Ou seja, ela pode começar a ser distribuída instantaneamente.”
Velho normal só no fim de 2021
O impacto das vacinas contra a covid-19 vai crescer rapidamente na metade do ano que vem, fazendo com que a vida volte ao normal até o próximo inverno no hemisfério norte, ou seja, no final de 2021.
A projeção foi feita por Ugur Sahin, co-fundador da alemã BioNTech, parceira da Pfizer. Segundo ele, o imunizante resultado da parceria pode evitar infecções, resultando em uma “redução dramática dos casos”. Em entrevista ao programa Andrew Marr Show, da TV britânica BBC, Sahin afirmou esperar que novas análises dos resultados da vacina apresentem tanto uma redução da transmissão do vírus, quanto um bloqueio ao desenvolvimento dos sintomas.
“Não devemos esquecer que, mesmo que a redução da transmissão seja de 50%, isso pode representar uma redução dramática na propagação da pandemia”. Testado em seis países, o imunizante é dado em duas doses, com três semanas de intervalo entre elas.
Segundo Sahin, é essencial que todos os programas de imunização sejam concluídos antes do próximo outono, que começa em setembro de 2021 no hemisfério norte. O executivo disse que ainda não se sabe quanto tempo dura a imunidade após a segunda dose da vacina ser aplicada.
Brasil sem previsão
Há dúvidas sobre uma eventual distribuição dela no Brasil. Em julho, a Agência Nacional de Vigilância Sanitária (Anvisa) liberou a realização do estudo clínico de fase três da vacina da Pfizer/BioNTech no País. Mas, até o momento, não existem conversas formais entre as duas empresas e o governo federal.
As farmacêuticas passaram ainda a negociar diretamente com governos estaduais. Se essas negociações forem bem-sucedidas (e a vacina aprovada), as primeiras doses só chegariam ao Brasil a partir dos primeiros meses de 2021. As entregas de 2020 já estão destinadas para outras partes do mundo.
Questionado se a vacina era tão eficaz em pessoas mais velhas quanto nas mais jovens, Sahin disse que terá essa resposta em breve. De origem humilde, o cientista é filho de um imigrante turco que trabalhava em uma fábrica da Ford em Colônia. Hoje com 55 anos, o presidente-executivo da BioNTech figura entre os 100 alemães mais ricos, junto com sua mulher e colega Öezlem Türeci, 53, filha de um médico turco.
J&J inicia novos testes
A Johnson & Johnson iniciou nesta segunda-feira um estudo de larga escala para testar um tratamento de duas doses de sua vacina contra covid-19, a fim de avaliar possíveis benefícios durante o período de proteção com uma segunda dose.
A farmacêutica norte-americana planeja recrutar até 30 mil participantes para o estudo e realizá-lo em paralelo a um teste de dose única, com até 60 mil voluntários que começou em setembro. O teste vem na esteira de resultados positivos do seu estudo clínico em andamento, de estágio inicial para intermediário, que mostrou que uma dose única induziu uma reação imunológica robusta e foi em geral bem tolerada.
*Com informações da Reuters